经典科幻电影中塑造的机械义体与生物体融合的半机器人,其超强力量、增强感知,以及电脑辅助大脑的高效信息处理能力,在生理和心理上极大地拓展了人类极限,展示出了具有巨大应用前景的人机协作未来。现阶段,构建半机械细胞(Cyborg cell)能否超越天然细胞,发展具有高度可编程的基因调控网络及定制化功能的智能细胞,具备更强大的信号感知及精准的基因操控能力,从而应用于基于合成生物学的疾病在体诊疗、生物医药生产等领域。
近日,华东理工大学生物反应器工程国家重点实验室叶邦策教授课题组在DNA传感装置的设计及生物纳米杂合系统研究中取得了重要进展,在国际权威期刊《美国化学会志》上发表了题为“Universal DNA-based Sensing Toolbox for Programming Cell Functions”的研究论文。该工作构建了纳米机械-天然杂合细胞,赋予了天然细胞非传统信号分子的感知、分析和处理能力,实现了多种生物功能的重编程。
运用基因工程手段重塑活细胞信号传感与通讯,实现高阶生理功能,应用于疾病诊疗领域,是合成生物学极具创新的概念之一。但基因工程本身安全性、通用性及天然细胞传感通路数量和结构的局限性制约其进一步发展。该工作通过构建细胞表面通用DNA传感工具箱,赋予细胞新型信号感知能力,控制细胞状态,实现多种细胞功能的重编程(图1)。利用DNA折纸三维结构作为基础框架,通过在其内部限域空间负载传感核心,不仅提高了工具箱在复杂生理环境中的稳定性,同时也增强工具箱的响应特异性和作用有效性。定制的感知核心配备多类型信号感知开关,拓展了非传统信号分子识别,配合功能性组分释放,实现对细胞凋亡、附着、激活分化、表达分泌等多种功能的调节控制,有望应用于免疫调节、疾病监测及肿瘤治疗等多种实用场景中。该工作通过构建纳米机械-天然杂合细胞,拓展了工程细胞感知信号和功能编程的多样性,为DNA传感装置的诊疗应用提供新策略,展示了纳米技术与生物系统相结合以创建先进感知和控制系统的新模式。
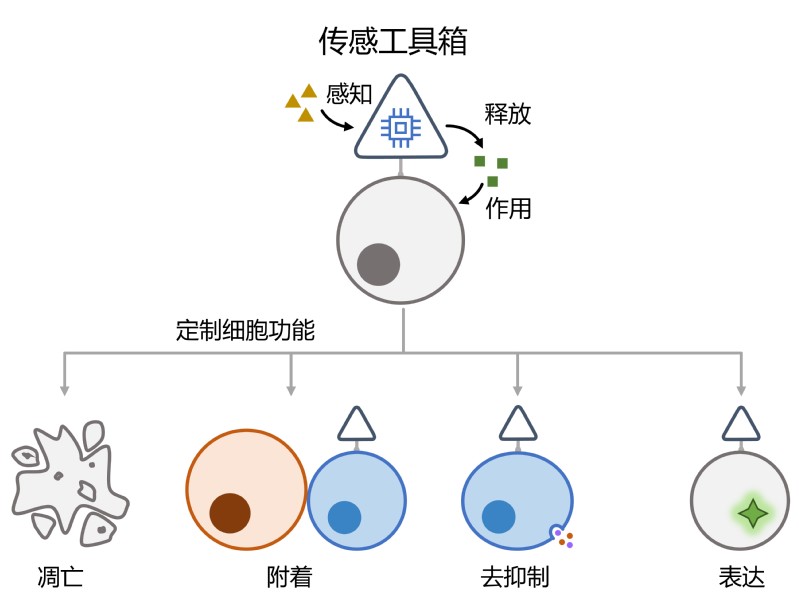
图1:通用型DNA传感工具箱定制细胞功能
近年来,叶邦策教授和尹斌成教授在DNA纳米装置设计及生物传感应用领域取得了一系列研究成果,利用纳米界面修饰及核酸可控组装技术,构筑了功能化传感界面,发展了新型运动机制、动力供给、轨道及动力组件设计,构建了一系列高性能DNA分子器件,应用于活细胞疾病相关分子丰度及其活力分析、基因调控、复杂生物运算、药物递送、多机器交互网络系统构建及免疫细胞工程改造等方面,为活细胞的高效信号感知及转换、基因调控网络重构及调节提供了设计新理念,拓展了核酸纳米装置的基础研究及生物医药应用(Small, 19, 2302301, 2023;Biosens.Bioelectron., 220, 114828, 2023;J. Am. Chem. Soc., 144,22458, 2022;Chem. Sci., 9, 3299, 2018;J. Am. Chem. Soc., 142, 3851, 2020;Talanta,215, 120898, 2020;ACS Appl. Bio Mater. 3, 2861-2866,2020;Angew. Chem. Int. Ed., 56, 9077, 2017)。
马培强副研究员和黄富文硕士为该论文共同第一作者,尹斌成教授为通讯作者。该研究得到了生物工程学院叶邦策教授的悉心指导与大力支持。该研究得到了国家重点研发计划、国家自然科学基金重点项目、上海生物制造产业协同创新中心重点项目、中央高校基本科研业务费专项资金等项目经费支持。
原文链接:https://pubs.acs.org/doi/full/10.1021/jacs.3c11232


