沙门氏菌(Salmonella)作为典型的食源性胞内致病菌,其致病性依赖于对宿主细胞内复杂环境的快速感知与适应性调控能力。在应对环境压力时,不仅依赖双组分系统介导的转录调控,还可通过翻译水平的动态调控实现更快速的应激响应。目前,关于原核生物如何通过翻译后修饰介导的核糖体异质性来调控蛋白质合成,并进而影响其致病能力的分子机制,仍缺乏明确证据。近日,华东理工大学生物工程学院、生物反应器工程全国重点实验室叶邦策教授团队在翻译后修饰调控病原微生物致病机理领域取得重要进展,相关成果发表于国际核酸研究领域权威期刊《核酸研究》。
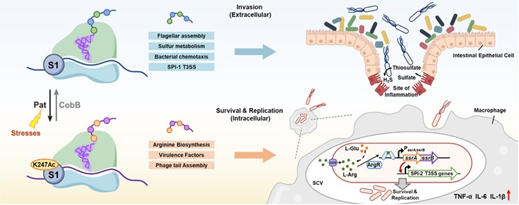
在该研究中揭示了一种新型的细菌毒力调控机制:鼠伤寒沙门氏菌通过动态调控核糖体蛋白S1的K247可逆乙酰化状态,实现翻译程序的精确重编程,从而适应宿主不同感染阶段的环境压力。研究证实,K247乙酰化由乙酰转移酶Pat和去乙酰化酶CobB动态调控。通过核糖体-新生肽链测序技术(RNC-Seq)分析,发现K247非酰基化状态倾向于结合鞭毛组装、硫代谢及SPI-1 T3SS相关mRNA,促进细菌早期侵袭能力;K247乙酰化则偏好性招募精氨酸合成及SPI-2相关mRNA,其中L-精氨酸可通过激活调控蛋白ArgR进一步上调SPI-2毒力因子的表达,从而增强细菌在巨噬细胞内的存活与复制能力。这一机制的发掘不仅阐明了病原菌利用翻译调控优化毒力表达的分子机制,也为开发针对核糖体翻译调控的新型抗菌策略提供了潜在靶点。
论文链接:https://doi.org/10.1093/nar/gkaf252


